Total Pengunjung Blog
Buku & Sastra Made Gue
All about CPOB
- download CPOB 2006 dan PCPOB 2009
- "catatan" dokumentasi berdasar CPOB
- Pets control berdasar CPOB 2006 serta implementasinya
- inspeksi diri dan audit berdasar CPOB 2006
- dasar - dasar kalibrasi alat
- Apa itu retain sampel BB dan produk jadi serta ongoing stabiliti?
- water treatment for pharmaceutical use
- Berbagai bentuk perawatan mesin industri farmasi dan pengertian downtime
- Apa itu retain sampel BB dan produk jadi serta ongoing stabiliti?
- Alat pengatur tekanan udara (magnehelic)
- instalasi pengolahan air limbah with aerob system
- Master requirment planning
- master production scheduling
- Cleaning validation
- 10 prinsip CPOB
- Validasi proses
- HVAC (Heating ventilation air conditioning
- water treatment in pharmaceutical industrion
- tata ruang industri farmasi beta laktam production & non betalaktam
- stability studi?
Penelitian & Kuliah
- Tips hemat dalam penelitian
- kristalisasi sederhana
- pelarut murni, perlukah untuk penelitian ?
- Cara memurnikan sampel yang jumlahnya sedikit ?
- Mendaur ulang silika bekas kromatografi kolom
- cara memilih hewan uji untuk penelitian
- Agar tak menjadi plagiat
- cara memilih solven untuk fase gerak KLT
- Pola data statistika yang sering di jumpai difarmasi
- tips mencari referensi ilmiah untuk mengerjakan tugas akhir
- Tutorial ms.word, mumudahkan menulis skirpsi (membuat daftar isi, page number, daftar pustaka
- Informasi seputar Beasiswa unggulan dan tips agar diterima
- Berbagai macam judul buku farmasi untuk referensi
- Cara download gratis jurnal berbayar maupun ebook
Daftar ISI
- DETERJEN (9)
- KOPI (24)
- PENELITIAN (16)
- PERISAI DIRI (12)
- PRIBADIKU (38)
- Sastra (98)
- Tips (24)
- computer and software (5)
- creative (18)
- dari blog friensdster (32)
- kuliah and buku (31)
- my BOOK (5)
- pascasarjana (43)
- profesi (45)
Pengikut
Popular Posts
-
Dear temen…kali ini andy lagi di tugasi oleh dosen untuk menulis 50 bahasa latin, gara =gara pretest andy g memenuhi kualifikasi.hehehe…...
-
Bagan alur ada di bawah….andy tampilkan di awal tulisan, agar nanti setelah membaca bagan bisa lebih paham.
-
PEMBALUT Pembalut tipis/plester of paris, sebelum pasien diberi pembalut gips, maka bagian tubuh tersebut diberi lapisan kapas gips yan...
-
Nama panjangku, Andy Eko wibowo, lahir pada tanggal 2 Juni 1988. Ayah bernama Dwi Yanto, dan Ibu bernama Retno Asih suminiati. Mempunyai dua...
-
Dear teman…..dear kawan-kawan sejawat farmasi dan kawan-kawan tercinta…meninjau kebutuhan teman-teman profesi terutama untuk yang angka...
-
Dear kawan kawan……..kali ini saya akan membagi pengalaman bagaimana MUDAHNYA mendapatkan beasiswa unggulan!!! sebelumnya, saya akan memberi...
-
Dear kawan…… Kali ini kita akan membahas mengenai bagaimana memilih fase gerak untuk kromatografi lapis tipis. Memilih solven sebagai ...
-
Dalam sebuah karya ilmiah baik itu sebuah penelitian maupun karya tulis tentunya para peneliti harus memiliki sumber referensi. Sumber refer...
-
Pada petunjuk CPOB 2009 Bab Bagunan dan Fasilitas, disebutkan bahwa untuk mencegah kontamination silang ( cross contamination) hendaklah dia...
-
sebelum menginjak ke pelayanan obat tanpa resep kita harus tahu terlebih dahulu apa itu obat tanpa resep??? klo obat dengan resep i...
Dear kawan..kali ini kita akan membicarakan gimana cara pembersihan di Industri agar nantinya produk tidak terjadi cross contamination.
Sebelum kita memulai validasi pembersihan atau cleaning validasi, alangkah lebih baik kita tahu terlebih dahulu, apa itu bersih?apa itu clean?? atau bahasa englishnya
“ how clean is clean??”
.
.
.
.
.
.
…………………………….bisa jawab???
jadi bersih itu ada tiga aspek, secara visual, kimia, dan mikrobiologi. Untuk aspek yang terakhir untuk produk – produk steril harus nihil. Untuk Industri non steril boleh ada mikroba dengan batas yang ditentukan karena produk – produknya non steril.
Jadi cleaning validasi dilakukan agar semua tindakan pembersihan dapat menghasilkan kriteria dimana segala kontaminan berada dibawah kriteria yang diterima.
Cara menentukan bersih secara kimia gimana?
Permasalahan di pabrik adalah alat yang digunakan itu biasanya satu macam alat digunakan untuk berbagai macam produk, bahkan ada sampai 265 zat aktif di buat dalam satu alat. Nah, apabila kita tidak bersih maka dapat saja terjadi crosscontamination. lalu apakah kita akan memvalidasi kebersihan satu persatu dari 265 zat aktif tersebut ?? Kenapa bahan aktif bukan eksipien yang divalidasi?karena eksipien tidak menimbulkan masalah yang kritikal
Ternyata tidak.
Hal ini terjawab di CPOB 2006 Bab 12 Kualifikasi dan Validasi Sub bab Cleaning validasi 12.38 “Prosedur pembersihan untuk produk dan proses yang serupa dapat dipertimbangkan untuk memilih suatu rentang yang mewakili produk dan proses yang serupa. Satu studi validasi dapat dilakukan menggunakan pendekatan kondisi terburuk (worst case) dengan memerhatikan isu kritis”.
dengan adanya aturan ini maka dilakukan pendekatan dari ke 265 produk tersebut di breakdown dulu dalam berbagai kriteria :
1. Zat Aktifnya—>bahan aktif yang sama
2. Toksisitas
3. Kelarutan terhadap air
4. Frekuensi manufacture
Kenapa kelarutan terhadap air masuk ke perhitungan???
Menurut CPOB 2006 pada Bab 5 Sanitasi dan Higiene sub bab pembersihan dan sanitasi peralatan (5.25) halaman 34 mengatakan bahwa “metode pemberishan dengan cara vakum atau cara basah lebih dianjurkan. Udara bertekanan dan sikat hendaklah digunakan dengan hati – hati dan sedapat mungkin dihindari karena menambah resiko pencemaran produk”.
Jadi untuk itulah kelarutan terhadap air dimasukkan disamping alasan penggunaan larutan organik sangat dihindari karena mudah menguap dan belum resiko mudah terbakar.
Lalu setelah di break down, kita mulai menggunakan skor pada masing – masing bagian dari no 2 sampai 4 untuk zat aktif yang berbeda.
| Kriteria | parasetamol | siprofloksasin | ctm |
| Toksisitas | 2 | 9 | 3 |
| kesukaran larut | 7 | 7 | 4 |
| Frekuansi manufacture | 10 | 2 | 3 |
| jumlah | 19 | 18 | 10 |
dengan demikian zat aktif dari 265 produk memiliki skor masing masing yang kemudian skor tertinggi akan digunakan. Misal produk Parasetamol dominan, maka parasetamollah yang akan digunakan sebagai indikator.
Misal Rangkaian alat produksi terdiri dari mixing, wetting, sluging, granulating, mixing, dan filling.
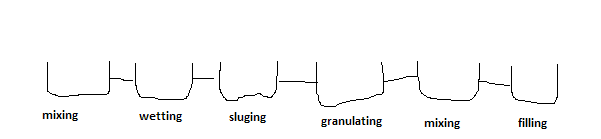
klo skor zat aktif ada yang sama tingginya. Misal ada 5 produk yang dijalankan pada mesin memiliki skor tertinggi, maka bagian mana yang akan kita pilih sebagai indikator??
maka jawabannya adalah zat aktif yang dipilih sebagai indikator adalah zat aktif yang memiliki cara pendeteksian paling mudah. Mudah dalam artian cepat, peka, dan prosedur mudah.
oh iya, intermezzo, berdasarkan CPOB pada Bab Kualifikasi dan Validasi sub bab Cleaning validasi halaman 120 no 12.36 mengatakan bahwa “hendaklah digunakan metode analisis tervalidasi yang memiliki kepekaan untuk mendeteksi tingkat residu atau cemaran yang dapat diterima”
berdasarkan kenyataan tersebut, maka alat yang digunakan sangatlah peka karena yang diukur adalah residu seperti AAS, GC, maupun HPLC dan alat – alat lainnya.
Dari sini dapat mengambil kesimpulan bahwa semua alat produksi minimal harus mempunyai 1 indikator yang digunakan untuk Cleaning. Ada Industri yang menggunakan minimal dua indikator dengan alasan karena lebih aman dan tangguh.
Lalu, sampai batas mana kriteria penerimaan/limit alat deteksi yang digunakan sehingga cemaran bisa dikatakan terkontrol bersih. Hal ini dapat dijawab dengan dua literature :
1. 10 ppm –>pada batas kurang dari 10 mg produk A diperbolehkan di 1 kg produk B.
2. 0,1 % dr TDD (teraupetik dari dosis).
kedua batas penerimaan tersebut disebut MACO (Maksimum Allowble curry over)
lalu dari parameter tersebut, batas mana yang diambil??Batas yang diambil adalah nilai yang paling kecil. Hal ini dikarenakan kita mendeteksi analite yang berupa residu.
Berkaitan dengan validasi kebersihan , kita juga harus patut menanyakan metode pengambilan sampling, bagaimanakah??
Cara pengambilan sampling ada 3, yakni :
1. Swab
2. Rinse
3. placebo
Untuk metode placebo tidak dianjurkan dikarenakan kurang reprodusible. Sedangkan untuk swab dan rinse lebih dianjurkan.
Untuk metode swab dengan cara menswab langsung menggunakan alat yang langsung kontak dengan tempat mesin yang akan divalidasi. alatnya seperti pengorek telinga tapi lebih agak besar. Alatnya ada dua jenis :

Cara menutulkan ke permukaan mesin produksi pun tiddak ada regulasinya, akan tetapi diharapkan putus – putus, karena menurut studi itu yang terbaik.
Untuk metode Rinse biasanya digunakan lebih ke peralatan yang besar. Meskipun demikian diwajibkan pula untuk mengkontrolnya menggunakan metode swab. Hal tersebut dikarenakan untuk produk –produk yang sukar larut air, apabila tidak digunakan metode swab maka tidak akan terdeteksi.
Ada dua jenis metode Rinse yakni :
1. Last Rinsing
2. Elution metode
Last rinsing menggunakan air terakhir yang ditampung volumenya dan di uji, sedangkan elution metode menggunakan pelarut alkohol yang ditampung (jarang dilakukan).
Menggunakan Swab adalah :
1.yang sukar larut bisa terdeteksi
2. di alat mixing cairan tidak ada maximum volume, sehingga ada lokasi yang menumpuk residu bahan aktif.

intermezo :
aturan tempat pengambilan sample pada cleaning validation adalah pada tempat yagn sulit dibersihkan.
CIP –>cleaning in place, sistem sistem pembersihan sendiri
SIP –>sterile in place. minim kontak dengan orang
Nah…setelah tahu cara pembersihan, kita sekarang belajar mengenai validasi metode analisis residu yang akan kita gunakan untuk membersihkan residu tersebut.
Validasi metode analisis
VMA dibagi menjadi dua bagian, yakni :
1. Spesifik (Direct Methode), contohnya adalah metode analisis yang menggunakan AAS, HPLC, GCMS
2. non spesifik (indirect methode) contohnya adalah metode analisis yang hanya dengan mengecek pH-meter, conduktivity,
Karena yang kita ukur adalah residu maka kita harus sangat memperhatikan LOD (limit of detection). Dengan demikian kita harus memilih alat yang sesuai. Jadi, untuk metode analisis pada validasi kebersihan lebih dipilih direct methode. Jika tidak bisa, baru kita pilih metode non spesifik.
Pada cleaning validasi, setelah semuanya lengkap, baik metode analisis, indikator, peralatan, kriteria penerimaan baru kita membuat protokol validasi. selanjutnya adalah tahap eksekusi dimana nanti bentuk dokumentnya dalam bentuk laporan pelaksanaan validasi kebersihan.
intermezzo…
dalam validasi dikenal TACT. Yakni Time, Action, Concentration, dan Temperature . Harus jelas waktunya berapa menit, pelaksanaannya disikat, atau direndam, atau di vakum, konsentrasi pembersih seberapa, dan suhu menggunakan air dingin atau air panas.







8 komentar:
Keren abis...
Coba dong buat alur produksi semua lini, mulai dari solida (betalaktam non betalaktam) kalo ada yang salut n SR(sustained released) terus steril, liquid, alur dari bahan di PPIC ad jadi produk jadi yang siap di jual di pasaran...tks riwa
wah 2 kata to itheng cemani "Detail dan Simple"......good! disertai pembahasanya.
terima kasih...
pak andi, punya contoh protokol validasi pembersihan alat diindustri? sebagai referensi tugas...
ebooknya ada mas, klo protokolnya sya blum nyari...
Pak andi, untuk kosmetik bagaimana cara menentukan kriteria penerimaannya ya? dan untuk VMA nya apakah diperlukan sampai menggunakan HPLC dll? apakah ada ebook nya untuk validasi cleaning nya kosmetik? thanks
Malam, maaf mau tanya. bagaimana cara menentukan kriteria penerimaan mikro ny yah..??? dan pedomannya dari buku apa..??makasih
Malam, maaf mau tanya. bagaimana cara menentukan kriteria penerimaan mikro ny yah..??? dan pedomannya dari buku apa..??makasih
Posting Komentar
komentari dunk....(tapi maaf ya...karena banyak spam yang masuk, maka saya harus terpaksa memunculkan verifikasi kata)